Der niedergelassene Chirurg
 Zeitschrift für Chirurgie in der Praxis – Nov. 1999
Zeitschrift für Chirurgie in der Praxis – Nov. 1999
Originalartikel
Externe Valvuloplastie (EVP),
Venenklappenkorrektur nach Dr. Tavaghofi im
Vena-saphena-magna-System als schonende und venenerhaltende Therapie
A. Tavaghofi
Zusammenfassung:
Die externe Valvuloplastie (EVP) ist eine schonende, venenerhaltende, alternative phlebo-chirurgische Methode besonders bei der Varikose im Venasaphena-magna-System. Ziel ist es, die defekten Venenklappen wieder funktionstüchtig zu machen und einen Kompressionsstrumpf von „innen“ zu ergänzen oder zu ersetzen.
In den letzten Jahren haben wir über 10.000 Beine (70 % Frauen zwischen 30 und 78 Jahren) zusätzlich zu den anderen üblichen Methoden oder allein durch EVP behandelt.
Postoperative Kontrolluntersuchungen und Auswertungen über einen Zeitraum von elf Jahren (1985-1996) bestätigten die Effizienz der Methode. Die Rezidivrate lag bei 11,49 %, wobei die echten Rezidive mit 3,8 % im Bereich der Vena saphena magna jedoch außerhalb der EVP-behandelten Strecken lagen, und 7,69 % (die unechten Rezidive) Seitenastvarizen darstellten, die mini-phlebo-chirurgisch nachbehandelt wurden.
Summary
External valvuloplasty (EVP) represents a smooth alternative method, specially with regard to the surgical treatment of the saphenaus vein varicosis. Task and target is to repair the insufficient valves, train them through EVP to become sufficient and replace from inside the function of compression stockings (internal compression stocking).
In the last 17 years we treated over 10,000 legs (70 % women between 30 and 78 years old), added to other usual methods or through EVP alone.
The postoperative studies of measurements and results of 11 years could prove the efficiency of this method. The recidives over those years were 11,49%: 3.8 % in the area of EVP-treated Vena saphena magna, and the rest (7,69 %) were reticular verikose which could treated through mini-surgical methods.
Einleitung
Auf den großen phlebologischen Kongressen waren in den letzten Jahren folgende Tendenzen zu erkennen:
- Zurückhaltung bei der Radikalphlebochirurgie wie Stripping
- zunehmend wissenschaftliche Berichte über venenerhaltende Maßnahmen wie externe Valvuloplastie (EVP).
Der hinter dieser Korrekturoperationstechnik stehende Gedanke ist über 25 Jahre alt und einfach. Der tiefe Venenbaum ist ausreichend von „Stützmaterial“ aus Knochen und Muskeln umgeben und somit varikös wenig anfällig. Die Vena saphena magna (VSM) ist jedoch von Fett umgeben, von Haut überzogen und größerem Druck ausgesetzt.
Wenn die Venenwand durch verschiedene Einflüsse (erblich, mechanisch, thermisch, chemisch) varikös verändert ist, die Zipfelklappen undicht werden und unter dem Staudruck und der Erdanziehung umkehren, entsteht zwischen den Zipfelklappen eine Lücke. Dadurch fließt die hochgepumpte Blutsäule (Muskelpumpe) beim stehenden Menschen im gleichen Augenblick zurück. Die Zipfelklappen schlagen distal um, degenerieren oder verkleben mit der defekten Venenwand. Es gilt also, durch die EVP die Lücke zwischen den defekten Klappen zu verkleinern oder zu schließen.
Bei den ersten Versuchen vor rund 20 Jahren haben wir einen inkompletten Fadenring aus Mersilene etwa 10 mm distal der defekten Klappe ambulant operativ angebracht, die Venenwand um etwa 30 % eingeschnürt und somit die Lücke zwischen den defekten Zipfelklappen verschwinden lassen.
Der in Lokalanästhesie operierte Patient berichtete unmittelbar nach dem Eingriff über die sofortige Entlastung des Beines („leichtes Bein“), ja sogar über Beschwerdefreiheit. Er hatte eben einen „inneren Kompressionsstrumpf‘ erhalten, der selektiv auf die VSM einwirkte.
Einige Jahre später haben wir wegen der besseren Hämodynamik zwei inkomplette Ring-Ligaturen distal der defekten Klappe im Abstand von etwa 5-8 mm operativ eingesetzt und die VSM zylindrisch eingeengt
(EVPTechnik, University of Sassari, Italy, [1]).
Seit etwa acht Jahren setzen wir einen größeren Proximal- und kleineren Distalring ein und bilden dadurch einen kleinen Trichter unterhalb der defekten Venenklappe. Die Hämodynamik ist nach dem physikalischen Gesetz von Laplace und wegen der veränderten Flußrichtung des Blutes an der Trichterwandung noch günstiger. Durch den Düsenstrahleffekt werden die umgestülpten Venenklappen in die physiologische Richtung zurückgedrängt. Die gleiche Technik findet auch Anwendung im Bereich der Perforansvenen.
Die EVP hat gegenüber den radikaloperativen Methoden Vorteile:
- Erhaltung der VSM für einen eventuellen aorto-koronaren Bypass
- Keine endgültige Situation; keine Überlastung der tiefen Vene und dadurch bedingte Pseudorezidivbildung.
- Vermeidung der nicht seltenen Verletzung der Äste des Nervus saphenus (Parästhesie!).
- Geringer Operationsaufwand für den Operateur und den Patienten; ambulant sehr gut durchführbar; mit entsprechender Geräteausstattung, auch ohne Assistenz.
- Kaum körperliche Belastung für den Patienten durch den Wegfall der Vollnarkose. Gut geeignet für Risikopatienten (kardial, renal usw.).
- Wegfall der Arbeitsunfähigkeitsund Krankenhaustage und dadurch erhebliche Kostenersparnis für Versicherer, Arbeitgeber und nicht zuletzt auch für den Patienten.
Methodik
Diagnostik, Effizienz und EVP-Simulation:
Bei der primären VSM-Stammvarikose werden die defekten Klappen im Bereich der VSM präoperativ durch aszendierende „Preß-Phlebographie“ dargestellt und auf den Ganzbeinröntgenbildern durch Vergleich und Messung bei der Untersuchung ausgewertet. Die Stellen der Klappen werden beim stehenden Patienten auf der
Haut im VSM-Bereich mit einem wasserfesten Stift markiert. Durch die Phlebographie haben wir eine exakte Aussage über den tiefen Venenbaum als Voraussetzung für die EVP.
Präoperativ sind dokumentativ noch durchzuführen:
- Digitale Photoplethysmographie (D-PPG)
- Venenverschluß-Plethysmographie (VVP)
- Reaktive Hyperämie
- CW-Doppler, Arterien-Nenenprofil
- Farb-Duplex-Untersuchungen
- Phlebodynamometrie (PDM)
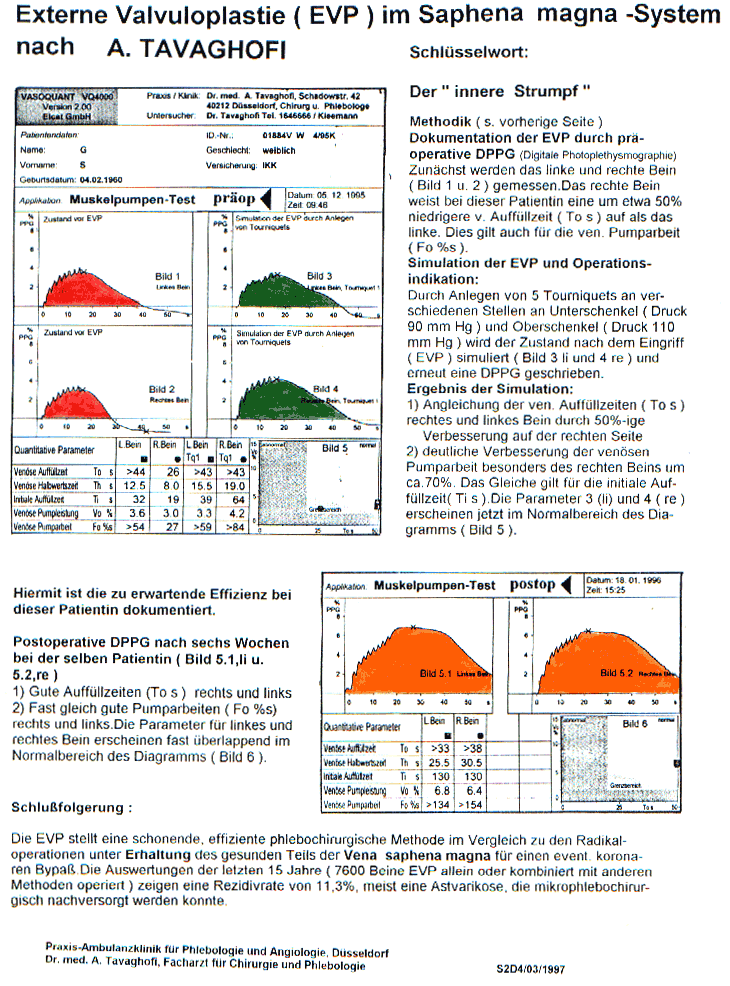
Erfahrungsgemäß liefert die präoperative, simulative D-PPG den Beweis für die Effizienz der EVP, Tabelle 1 zeigt die Daten eines Patienten. Im Vergleich links zu rechts sieht man eine deutliche Differenz der venösen Auffüllzeit (T os) und eine erhebliche Differenz der venösen Pumparbeit (links 54 %s, rechts 27 %s).
Die Operationsindikation zur EVP wird durch das Anlegen von fünf Tourniquets an folgenden Stellen simuliert:
- 10 cm oberhalb des Innenknöchels
- Wadenmitte
- dickste Stelle des Unterschenkels
- Handbreit oberhalb des Kniegelenkes, am Unterrand des Adduktorenkanals
- eine Handbreit unterhalb der Leistenfalte
- (Druck Unterschenkel etwa 120, Oberschenkel etwa 160 mmHg)
Es wird eine simulative D-PPG angefertigt.
Tabelle 1 zeigt einen Angleich der venösen Auffüllzeit und den Anstieg auf links und rechts 43 s (To) – eine Verlängerung der venösen Auffüllzeit um 100%. Die Pumparbeit ist rechts um 70% gebessert. Gleiches gilt für die initiale Auffüllzeit (Ti).
So kann man prä-EVP von einem Behandlungserfolg ausgehen.
Derselbe Patient erzielt sechs Wochen nach EVP gute Ergebnisse (Tabelle 1):
1. Angeglichene Auffüllzeiten (To) rechts und links 33/38 s
2. Deutlich gesteigerte Pumparbeit rechts und links (Fo 134/154 %s)
Verfahrenstechnik
Technische Hilfsmittel und Spezialinstrumente
(alle nach A. Tavaghofl) für die EVP:
– Gefäßuntersuchungsstuhl
– Gefäßoperationstisch
– Phleb-Stringatoren mit Verengungsstufen von 1-5 und 2-7 qmm
– Phleb-Luxatoren
Durchführung der EVP:
- Präoperative Diagnostik, Phlebographie, Labor, EKG und Thrornboseprophylaxe nach ausführlicher und laienverständlicher Aufklärung des Patienten sowie der schriftlichen Einwilligungserklärung.
- Prämedikation: Atosil eine Ampulle i.m. eine Stunde vor dem Eingriff oder als „Drink“ 1,5 ml verdünnt mit 50 ml Wasser. Zeit zwischen Prämedikation und OP etwa zwei Stunden, damit die bestmögliche Relaxation zwecks Hervorluxation der VSM erreicht ist.
- Markierung der Haut über den defekten Klappen, wie zuvor beschrieben, auf dem Untersuchungsstuhl im Stehen, mechanische Reinigung und Rasur der Haut im Bereich der Markierungen.
- Lagerung des Patienten auf dem Gefäß-OP-Tisch (je nach OP-Gebiet Seiten-, Bauch- oder Rückenlage).
Lokalanästhesie an den markierten Stellen zum Beispiel mit Xylocain 1 % ohne Adrenalin.
Achtung: Bei der Lokalanästhesie subkutan oder periversal bleiben! Gefäßwandverletzungen können Thrombosen verursachen und das so gebildete Hämatom kann die Anatomie verwischen.
Operationstechnik
Stichinzision (für VSM 5 mm, für Miniphlebochirurgie etwa 2 mm) möglichst 2 mm neben der Markierung (Tätowierungseffekt!). Von der Inzision aus wird mit dem kleinen Hakenende des Phleb-Luxators die VSM freipräpariert, hervorluxiert und auf den Stufenteil des Luxators gehoben. Das Gerät wird soweit vorgeschoben, bis die VSNI voll kollabiert. Durch die Kommissuren, die auftragen, können die Klappen erkannt werden.
Aus der Breite der kollabierten VSM, 7-15 mm distal der defekten Klappe in Millimeter gemessen, wird durch eine entsprechende Tabelle der Querschnitt der Vene im gefüllten Zustand ermittelt.
Beispiel: Bei einem Lumen von 10 qmm und einer gewollten 30%igen Reduzierung (damit sich die Lippen der degenerierten Klappen wieder berühren), wird der Teil des Stringators mit 7 qmm im Durchmesser (Stufe 3) zu Hilfe genommen und mit der linken Hand vom Operateur parallel neben die VSM auf den Luxator gelegt. Der Stringator wird dem Assistenten übergeben. Der Operateur unterfährt mit der rechten Hand mit einem Nadelhalter, bestückt mit einem atraumatischen Nahtmaterial (Polyvinylidendifluorid 4,0), die VSM und den Stringator gemeinsam (Abbildung 1). Der Faden wird jetzt etwa 5-8 mm distal der Venenklappe mit dem Inhalt Vena saphena magna und Stufe 3 des Stringators fest verknotet (Orientierungspunkt Kommissuren!)
Beim Unterfahren wird die Adventizia der Vena saphena magna vorsichtig etwas mitgenommen (ohne die Intima zu verletzen – Thrombosegefahr!) und der Ring so fixiert. (Achtung: Keine Nervenäste mit legieren!). Es entsteht der inkomplette Proximalring.
Gleiche Technik für die Bildung des Distalringes, jedoch 20 % kleiner im Querschnitt mit einem Abstand zum Proximalring von 5-10 mm je nach Kaliber der VSM. Nach Bildung von festen imkompletten Ligaturen werden Stringator und Luxator vorsichtig zurückgezogen und die VSM freigegeben, die sich füllt und die durch den Stringator vorgegebene Weite annimmt.
Die Spezialinstrumente sind deshalb erforderlich, weil man dann inkomplett und exakt nach Vorgabe knoten kann, wenn sich Material im Knoten befindet. Wiederholung des Vorganges je nach Zahl der defekten Klappen an anderen Stellen, anschließend Reposition der VSM und Verschluß der Haut durch eine feine Rückschichtnaht.
Ein Kompressionsverband ist nicht nötig (was der Patient als sehr angenehm empfindet), weil ein Hämatom wie bei den Radikaloperationen nicht zu erwarten ist.
Anmerkungen zur EVP-Operationstechnik:
- Damit die Vena saphena magna während der Operation gefüllt, tast- und sichtbar ist, bleibt das am Oberschenkel angelegte Tourniquet oder die Pumpmanschette während der gesamten OP-Zeit geschlossen.
- Die EVP als extraluminales operatives Geschehen ohne Verletzung der Intima wirkt wie ein Kompressionsstrumpf eher antithrombotisch. Sie kann auch problemlos bei Marcumar-Patienten angewendet werden. In den letzten elf Jahren haben wir über 100 Marcumar-Patienten komplikationslos mit EVP behandelt.
Bei EVP handelt es sich meist um eine etagenweise Korrektur-OP der VSM. Als Thromboembolieprophylaxe, insbesondere bei älteren Patienten (Tendenz zur Immobilität!), ist die s.c. Injektion von niedermolekularem Heparin, 0,5 ml Ampulle, alle 24 Stunden für etwa 8 Tage zu empfehlen.
Langzeit-Ergebnisse
Die prä- und postoperativen Vergleichsuntersuchungen, D-PPG, VVP, RH, CW-Doppler, Phlebographien und Farbduplex, belegen die gute Effizienz dieser schonenden und gefäßerhaltenden phlebo-chirurgischen Behandlungsmethode.
Die Auswertung von über 10.000 bei uns durchgeführten EVP’s in den letzten elf Jahren ergab eine Rezidivrate von 11,49 %. Dabei handelte es sich um 3,8 % echte Rezidive der Vena saphena magna -jedoch außerhalb der reparierten Strecke. 7,69 % waren unechte Rezidive, also Astvarikosen im Rahmen der chronisch-venösen Insuffizienz (CVI), die mikro-phlebo-chirurgisch gut behandelt werden konnten.
Die meisten Patienten berichteten nach dem ersten oder zweiten Eingriff über eine deutliche Erleichterung oder sogar das Verschwinden der Beschwerden. Die prä- und post-EVP-Phlebographien zeigen die deutlich schlank gewordene VSM und das Verschwinden der Varizen (Abbildung 2, zwei verschiedene Patienten). Sechs Monate nach der EVP konnten bei 30% der präoperativ geröntgen Beine durch eine deszendierende Phlebographie die physiologische Klappenfunktion nachgewiesen werden. Die prä- und postoperativen Farbduplex-Untersuchungen bestätigen die phlebographischen Ergebnisse. Letzterer Phlebographie ist eine größere Präzision und Sicherheit zuzuschreiben.
Nicht nur die postoperativen Meßergebnisse sind ein Parameter für den Operationserfolg, sondern auch, was die Patienten uns Jahre nach der Operation berichten. Die prä- und postoperativen Dokumentationsfotos (Abbildung 3) belegen gute kosmetische Ergebnisse, was die Patientinnen besonders freut.
Schlußfolgerung
Die operative Therapie der VSM-Stammvarikose geht in den letzten Jahren international, besonders in den USA, in Richtung der schonenden und venenerhaltenden Eingriffe wie zum Beispiel der EVP. Es gibt keine endgültig heilende, operative Varizen-Behandlungsmethode. Die CVI ist fast immer dabei und der Venen-Patient bleibt oft behandlungsbedürftig. Die EVP stellt jedoch, nach jahrelangem Einsatz und Erfahrungen, eine mini-inversive phlebo-chirurgische Alternativmethode dar, um dem Patienten über einen größeren Zeitraum zu helfen.
Motto: „Zuerst reparieren und Zeit gewinnen, statt sofort zu entfernen!“
Es wurden noch um die 80 Veröffentlichungen für Fachzeitschriften, Ärztekongresse und andere Fachinformationen von Dr. Tavaghofi herausgegeben.